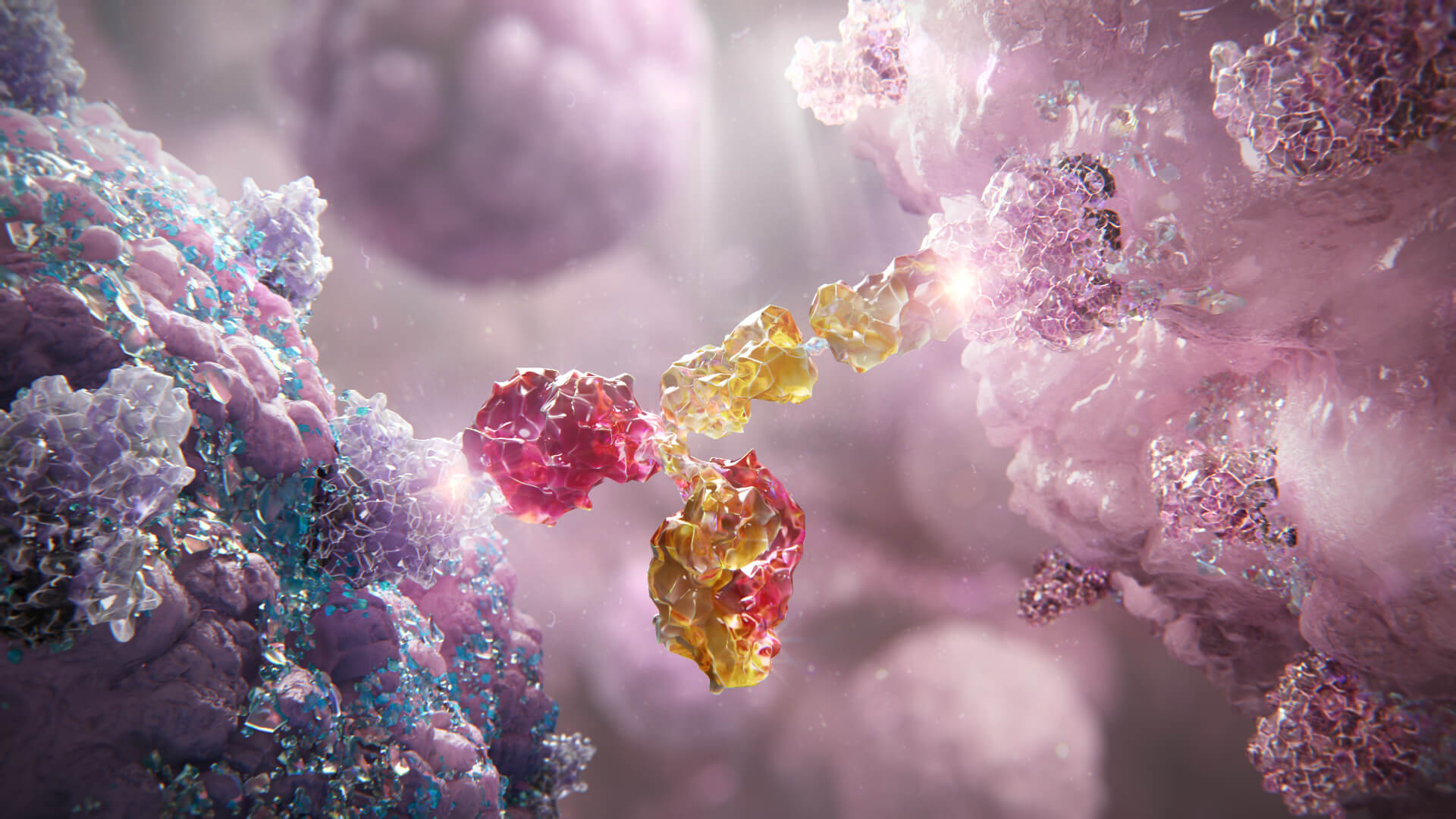
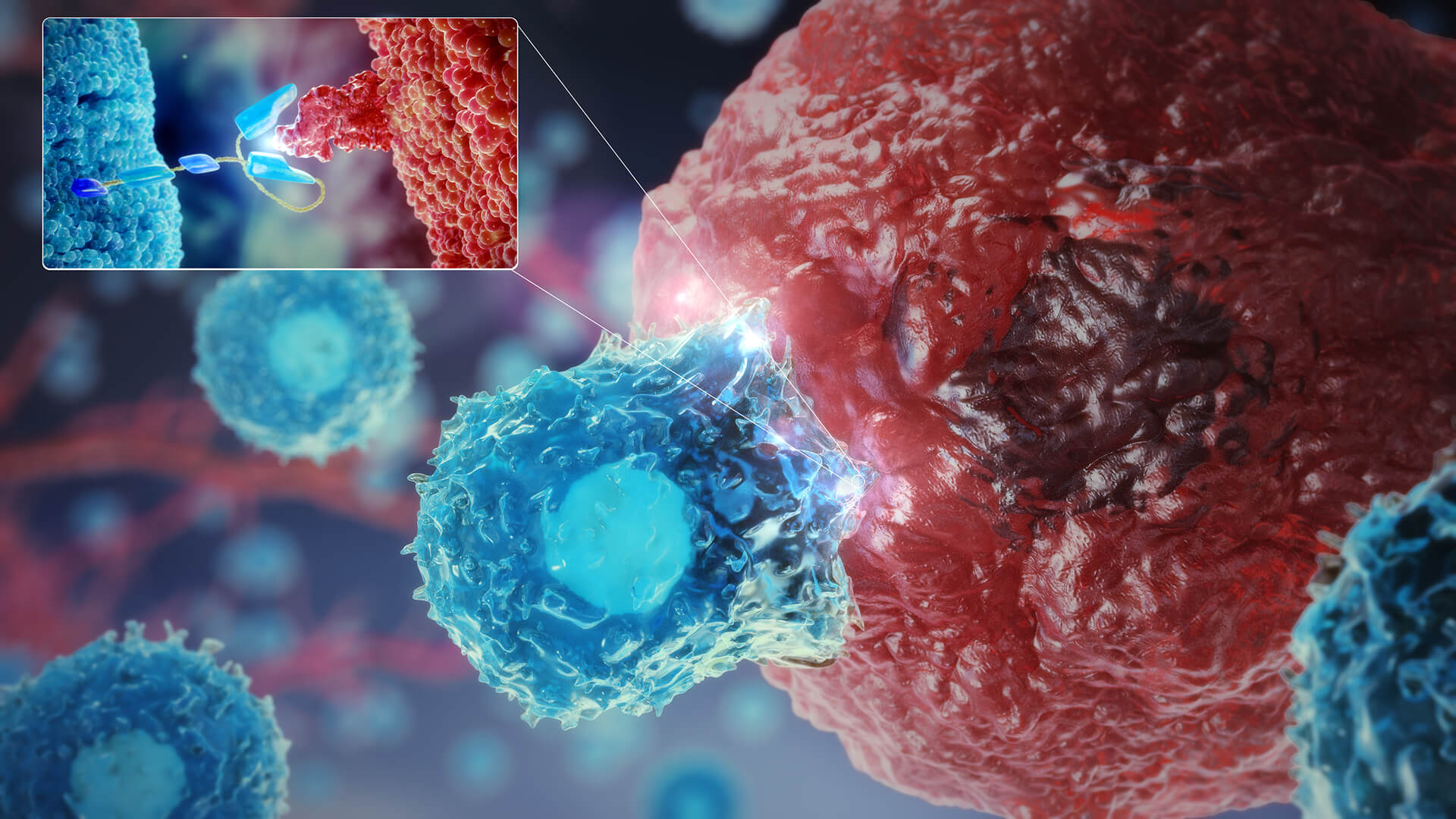
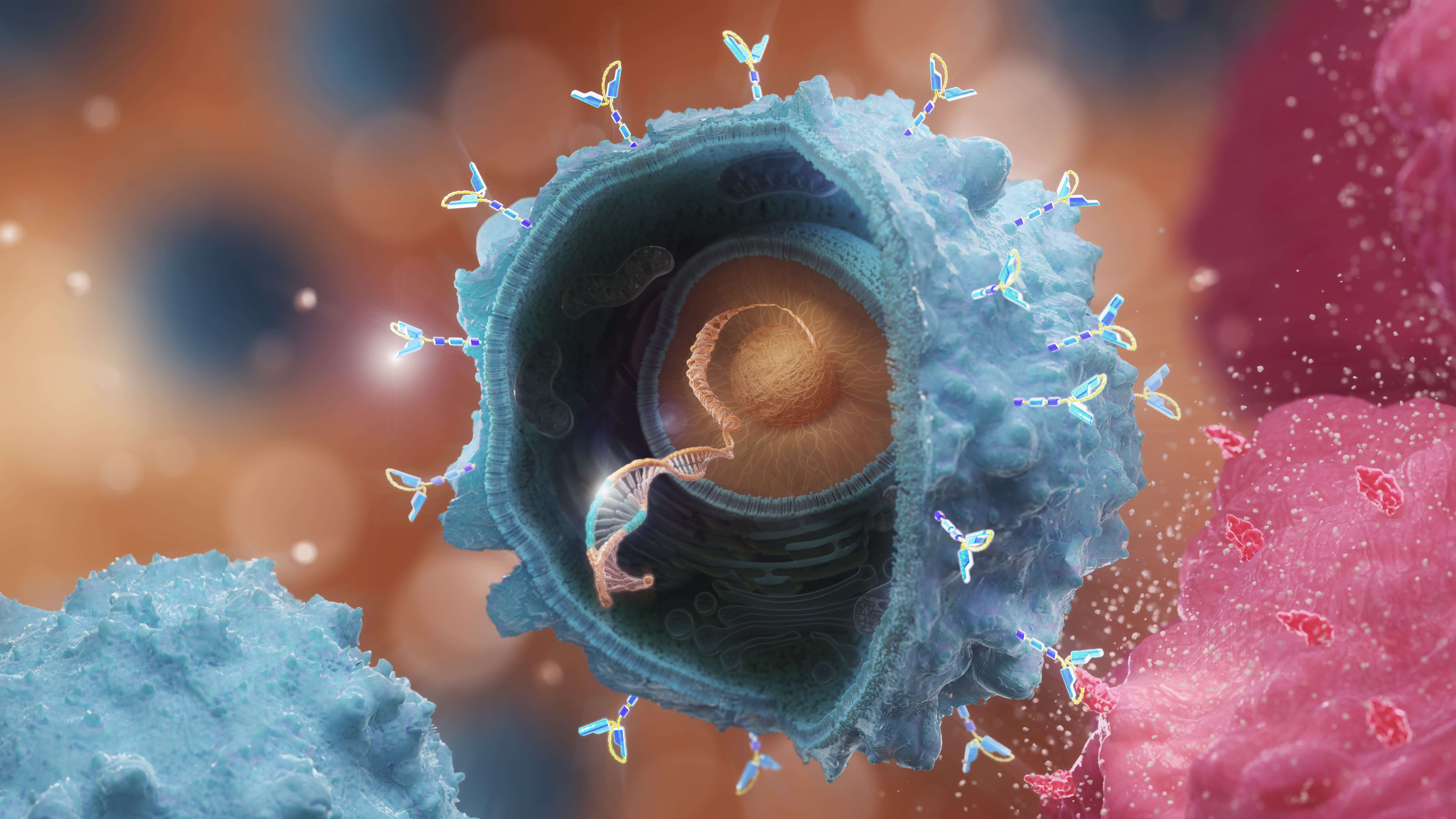
CAR-T (Chimeric Antigen Receptor T-cell — Т-лимфоциты с химерным антигенным рецептором) терапия, как и другие клеточные технологии, является одним из самых современных подходов в терапии злокачественных опухолей. При ее проведении у пациента забирают Т-лимфоциты и внедряют в их ДНК участок, который имеет химерный антигенный рецептор (CAR).
Он помогает выявить антиген на мембране опухолевой клетки, то есть распознать ее. Затем эти модифицированные Т-клетки иммунитета возвращают в организм, и они становятся опухолевыми киллерами.